Сертификация ГОСТ Р ИСО 13485-2017 (ISO 13485:2017) в Москве
Система менеджмента качества производителей медицинских изделий
Оформление сертификата ГОСТ Р ИСО 13485-2017
ISO 13485 – международный стандарт, содержащий требования к системе менеджмента качества производителей медицинских изделий. Эти требования являются дополнительными по отношению к техническим требованиям к продукции. Основой для разработки ГОСТ ISO 13485 явился стандарт EN 46001 «Quality systems — Medical devices — Particular requirements for the application of EN 29001» (введен в действие в 1993 году и отменен в 2000 году).
Начиная с 01.03.2019 органы по сертификации, имеющие аккредитацию на проведение сертификации ИСО 13485, будут проводить оценку организаций согласно требованиям новой редакции стандарта.
Порядок прохождения сертификации за 1-5 дней в Москве:




В стоимость включено
- Персональный эксперт
- Внесение в Единый реестр
- Сертификат соответствия
- Сертификаты на сотрудников организации
- Разрешение на применение знака соответствия
- Дальнейшее юридическое сопровождение
Мы зарегистрированы в государственном реестре
Организация «НОПСС» зарегистрирована в едином реестре Федерального агентства
по техническому регулированию и метрологии Росстандарт за номером РОСС RU.З2449.04НОП03.
Ссылка на реестр РОССТАНДАРТА GOST.RU.
Требования к сертификату от заказчика, тендерной комиссии и СРО
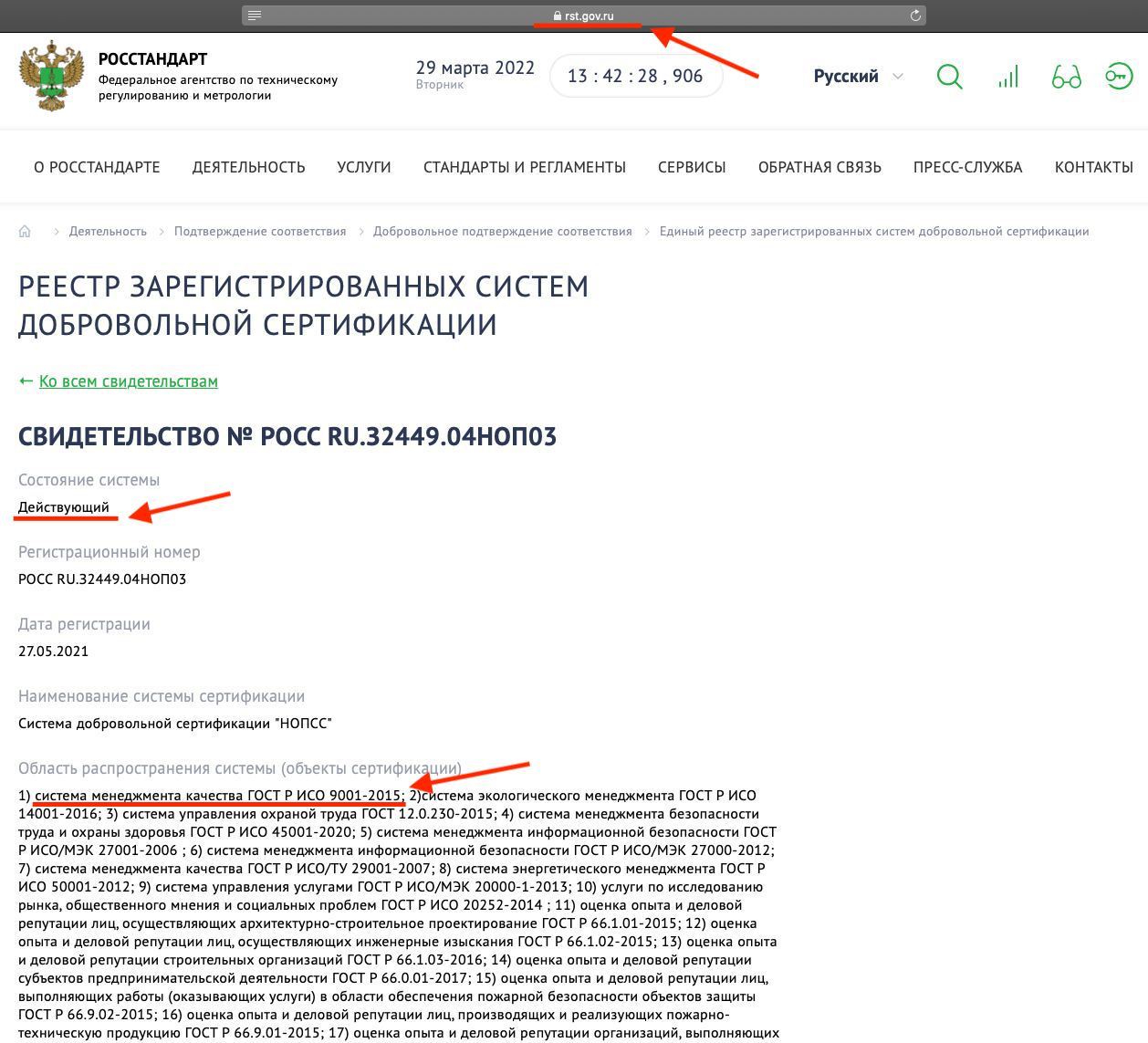
Перед получением сертификата убедитесь, что система добровольной сертификации соблюдает следующие требования:
- Система добровольной сертификации должна быть зарегистрирована в реестре Росстандарта на официальном сайте;
- Состояние системы должно иметь статус «действующий»;
- В области распространения системы должен быть стандарт по выданному сертификату в следующем виде: расшифровка стандарта, номер стандарта, например: «система менеджмента качества ГОСТ Р ИСО 9001-2015».
Внимание! Большинство стандартов имеют несколько версий, в зависимости от года. Например: ГОСТ Р ИСО 9001-2008, ГОСТ Р ИСО 9001-2011, ГОСТ Р ИСО 9001-2015. Отсутствие номера стандарта (9001-2015) в реестре, не дает возможность проверить законность выданного сертификата по причине отсутствия года (2015). В связи с этим, сертификат может быть отклонен.
Получите предварительный расчёт стоимости сертификации за 1 минуту
Возникли вопросы?
Оставьте свои контакты, и наш менеджер поможет вам в течение пяти минут.
Cистема менеджмента качества медицинских изделий
Стандарт определяет требования к системе менеджмента качества медицинских изделий. Они должны применяться организацией при проектировании, разработке, производстве, монтаже и обслуживании медицинских изделий, а также при проектировании, разработке и обеспечении связанных с ними услуг.
Требования стандарта идентичны требованиям ISO 9001, но имеются отличия, учитывающие особенности медицинской отрасли:
- специальные требования к стерильным медицинским изделиям;
- валидация всех процессов производства и обслуживания;
- идентификация и прослеживаемость;
- специальные требования к активным имплантируемым медицинским изделиям;
- сохранение соответствия продукции;
- управление устройствами для мониторинга и измерений;
- более жёсткая система требований, касающихся валидации, управления производством, метрологического обеспечения, управления персоналом, документирования;
- отсутствуют требования демонстрации постоянного улучшения — ГОСТ ISO 13485-2017 требует, чтобы сертифицированная организация демонстрировала, что система качества эффективно внедрена и поддерживается;
- отсутствуют требования к оценке удовлетворенности потребителей;
- стандарт предполагает больший акцент на применении статистических методов, которые позволяют не только улучшать качественные показатели продукции, но и оптимизировать процесс.
Требования стандарта ИСО 13485 распространяются на организации, производящие медицинское оборудование и изделия и желающие поставлять свою продукцию в страны ЕС, занимающиеся проектированием и производством медицинской техники, разрабатывающие программное обеспечение.
Список необходимых документов:
Преимущества прохождения сертификации в нашей организации
Для чего необходим стандарт ISO 13485?
Наличие сертификата ИСО 13485 на медицинское изделие улучшает имидж компании, повышает доверие к продукции, укрепляет деловую репутацию. Требования стандарта ISO 13485-2017 распространяются на организации, предлагающие на рынок медицинские изделия, независимо от вида или численности этих организаций. НОПСС – это компетентный и квалифицированный персонал экспертов-консультантов, обладающих опытом разработки, внедрения и сертификации систем менеджмента по ISO 13485 медицинские изделия.
Прежде чем приступить к подготовке предприятия к сертификации в соответствии со стандартом 13485-2017 мы производим сбор данных, необходимый для формирования финансово оптимальной для Заказчика схемы работы. Партнерские отношения нашей организации с органами по сертификации могут привести к существенной экономии денежных средств по сравнению с аналогичными предложениями наших конкурентов.
Сертификат ИСО 13485-2017 – это стандартный специальный типографский бланк, содержащий информацию о заявителе, производителе, области действия СМК, дате начала и окончания срока действия, основаниях для выдачи. Документ содержит уникальный регистрационный номер и заверяется руководителем экспертной комиссии и руководителем органа сертификации, который его выдал. В течение всего срока действия сертификата организация должна проходить ежегодный контроль.
О нас в цифрах
 10 лет успешной работы на рынке
Многолетний опыт работы и высокое качество оказываемых услуг гарантируют надежность и доверие клиентов.
10 лет успешной работы на рынке
Многолетний опыт работы и высокое качество оказываемых услуг гарантируют надежность и доверие клиентов.
 12000 сертификатов выдано
Тысячи выданных сертификатов свидетельствуют о нашем профессионализме и эффективности.
12000 сертификатов выдано
Тысячи выданных сертификатов свидетельствуют о нашем профессионализме и эффективности.
 Официальная аккредитация
Легитимность нашей компании подтверждена, что гарантирует высокое качество выданных нами сертификатов.
Официальная аккредитация
Легитимность нашей компании подтверждена, что гарантирует высокое качество выданных нами сертификатов.
Наша команда
Наши партнёры


















Наши кейсы
Производственной компании, для заключения договора, нужно было получить сертификат безопасности труда и охраны здоровья. У компании не было денег, для получения аванса ей нужно было заключить договор.
После переговоров было принято решение заключить договор с отсрочкой платежа на 1 месяц.
После предоставленных документов, компания заказчика была внесена в единый реестр системы сертификации, сертификат был выпущен. Спустя 2 недели заказчик уже получил аванс, начал выполнение работ и оплатил прохождение сертификации досрочно.
Компании, оказывающей услуги в области налогового консультирования нужен был срочно сертификат ИСО 9001 в день обращения.
После получения документов было принято решение не дожидаться поступления оплаты и провести сертификацию вне графика.
Заказчик оплатил сертификацию, прислал платежное поручение с отметкой банка и организация «НОПСС» сразу же запустила процесс. Спустя 3 часа сертификация была выполнена в полном объеме. Компанию заказчика внесли в единый реестр системы, скан-копии документов отправили на электронную почту, а оригиналы доставили экспресс-курьером прямо в офис заказчика в этот же день.
Строительной компании, работающей на особо-опасных объектах нужен, был сертификат менеджмента качества для вступления в СРО
Было принято решение провести переговоры на предмет помощи в оказании услуг по вступлению в СРО. Вступая в СРО через аккредитованную организацию «НОПСС», компания получает сертификат ИСО 9001 в подарок.
Организацией «НОПСС» были бесплатно подготовлены все необходимые документы и сертификация ИСО 9001. Заказчик получил всю необходимую консультацию и оперативно вступил в СРО за 1 день.

Сертификация Системы менеджмента качества в здравоохранении ГОСТ Р ИСО 13485-2017 (ISO 13485:2017)
Организация «НОПСС» оказывает содействие медицинским организациям и предприятиям в Москве и по всей Московской области, занимающимся производством медицинского оборудования, оказанием услуг в этой сфере. Помогаем получить сертификат ISO 13485, подтверждающий, что компания может производить и поставлять на рынок товары, соответствующие предъявляемым к ним требованиям, удовлетворяющие запросы потребителей. Прохождение сертификации снижает риск выпуска некачественной продукции, улучшает методы контроля, повышает квалификацию сотрудников.
Преимущества добровольной сертификации ИСО 13485:
- расширение рынков сбыта продукции за счет стран ЕС и Таможенного Союза;
- рост конкурентоспособности;
- возможность участвовать в государственных закупках;
- привлечение инвестиций на развитие бизнеса;
- заключение выгодных контрактов;
- четкое выстраивание бизнес-процессов организации, эффективное распределение внутренних ресурсов, ответственности и полномочий персонала в рамках существующей системы менеджмента качества медицинских изделий.